1회 같은 성분, 다른 시장
인간의약품의 언어로 동물의약품 시장을 읽으면 안 되는 이유
아스피린은 개에게도 처방된다.
개의 항응고 관리나 근골격계 염증 완화에 수의사의 판단 아래 쓰이는 경우가 있다. 성분도 같고, 작용 기전도 같다. 그렇다면 자연스럽게 질문 하나가 떠오른다.
인간의약품과 동물의약품은 결국 같은 것 아닌가?
이 질문이 이 글의 출발점이다. 문제는 이 질문에 “그렇다” 고 답하는 순간, 인간의약품 시장의 지도를 그대로 들고 동물의약품 시장에 들어가게 된다는 점이다.
성분이 같다고 시장이 같은 것은 아니다.
왜 지금 이 이야기를 해야 하는가
지금 국내 제약업계는 동물의약품 시장으로 눈을 돌리고 있다. 유한양행은 반려동물 관절염 치료제 '제다큐어'를 시작으로 사료·진단 영역까지 사업을 확장하고 있고, 대웅제약은 당뇨 신약 '엔블로펫'과 아토피 피부염 신약인 '플로디시티닙'으로 신약개발에 속도를 내고 있다.
국내에서도 반려동물용 동물약품의 비중은 빠르게 커지고 있다. 업계 자료에 따르면 반려동물용 동물약품 판매 비중은 2018년 13%에서 2024년 26%로 확대됐다. 글로벌 시장 역시 반려동물 양육 증가, 예방의학 수요, 진단·디지털 헬스 확산을 배경으로 꾸준한 성장이 전망된다. 절대 규모는 인간의약품의 35분의 1 수준이지만, 시장이 작다는 것과 매력이 없다는 것은 전혀 다른 이야기다.
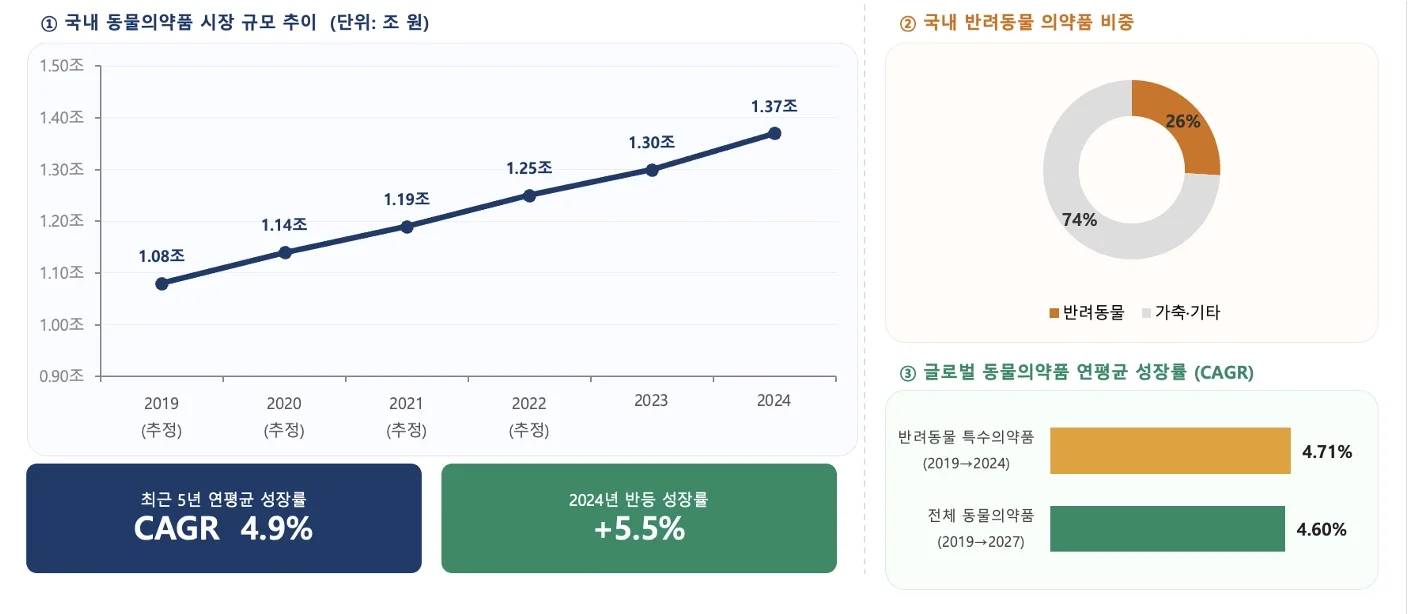
그림 1. 국내 동물의약품 시장 규모 추이 (출처: 국내 동물의약품 - 축산신문·농림축산검역본부)
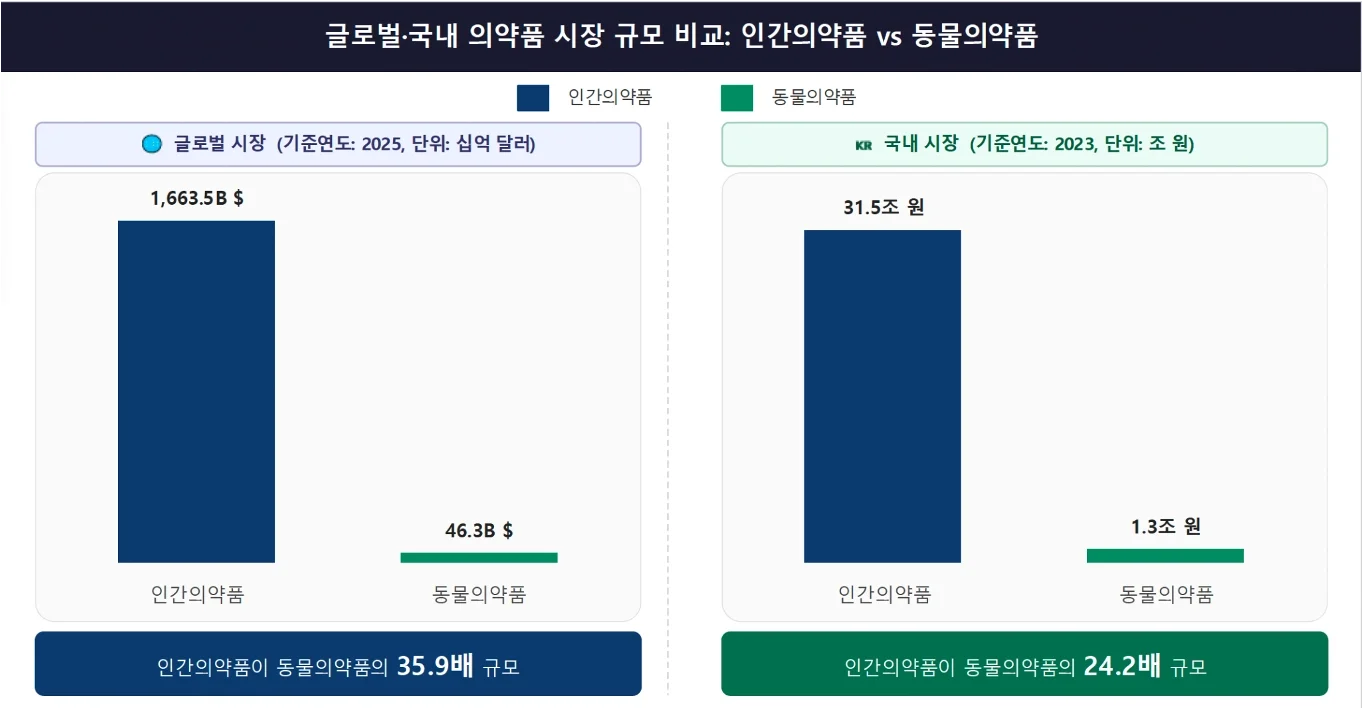
그림 2. 인간의약품, 동물의약품 시장 규모 비교: 글로벌 인간의약품 - Global Pharma Market Forecast 2025
글로벌 시장에서는 이미 수년 전부터 인간의약품 빅파마 내부에 있던 동물의약품 사업부가 독립 전문기업으로 분사했다. Zoetis는 Pfizer의 동물의약품 부문에서, Elanco는 Eli Lilly의 동물의약품 부문에서 각각 분사해 지금은 동물의약품 시장의 핵심 플레이어가 됐다. 국내 제약사들이 이 시장을 이제야 들여다보기 시작했다는 건, 기회이기도 하지만 동시에 더 늦기 전에 들어와야 하는 시장이라는 소리이기도 하다.
그리고 이 시장에 진입할 때 가장 많이 하는 실수가 있다. 익숙한 프레임을 그대로 들고 오는 것이다. 허가 절차는 유사하겠지, 임상 언어는 통하겠지, 가격 논리는 비슷하겠지. 이 가정들이 얼마나 빠르게 무너지는지 확인하는 데는 오래 걸리지 않는다.
같은 성분이라도 허가의 구조·단위가 다르다
그 가정이 가장 먼저 부딪히는 벽은 허가 구조다.
한국에서 인간의약품은 식품의약품안전처(MFDS)가, 동물의약품은 농림축산검역본부가 관할한다. 같은 성분이라도 동물용으로 쓰려면 별도 기관에 별도 기준으로 다시 허가를 받아야 한다. 이 구조적 차이는 개발 전략과 포트폴리오 설계 전반에 영향을 미친다. 두 시장의 허가 체계를 항목별로 비교하면 다음과 같다.
표 1. 인간의약품, 동물의약품 허가, 규제 체계 비교 (출처: 식품의약품안전처, 농림축산검역본부, VICH 가이드라인 기반 필자 정리)
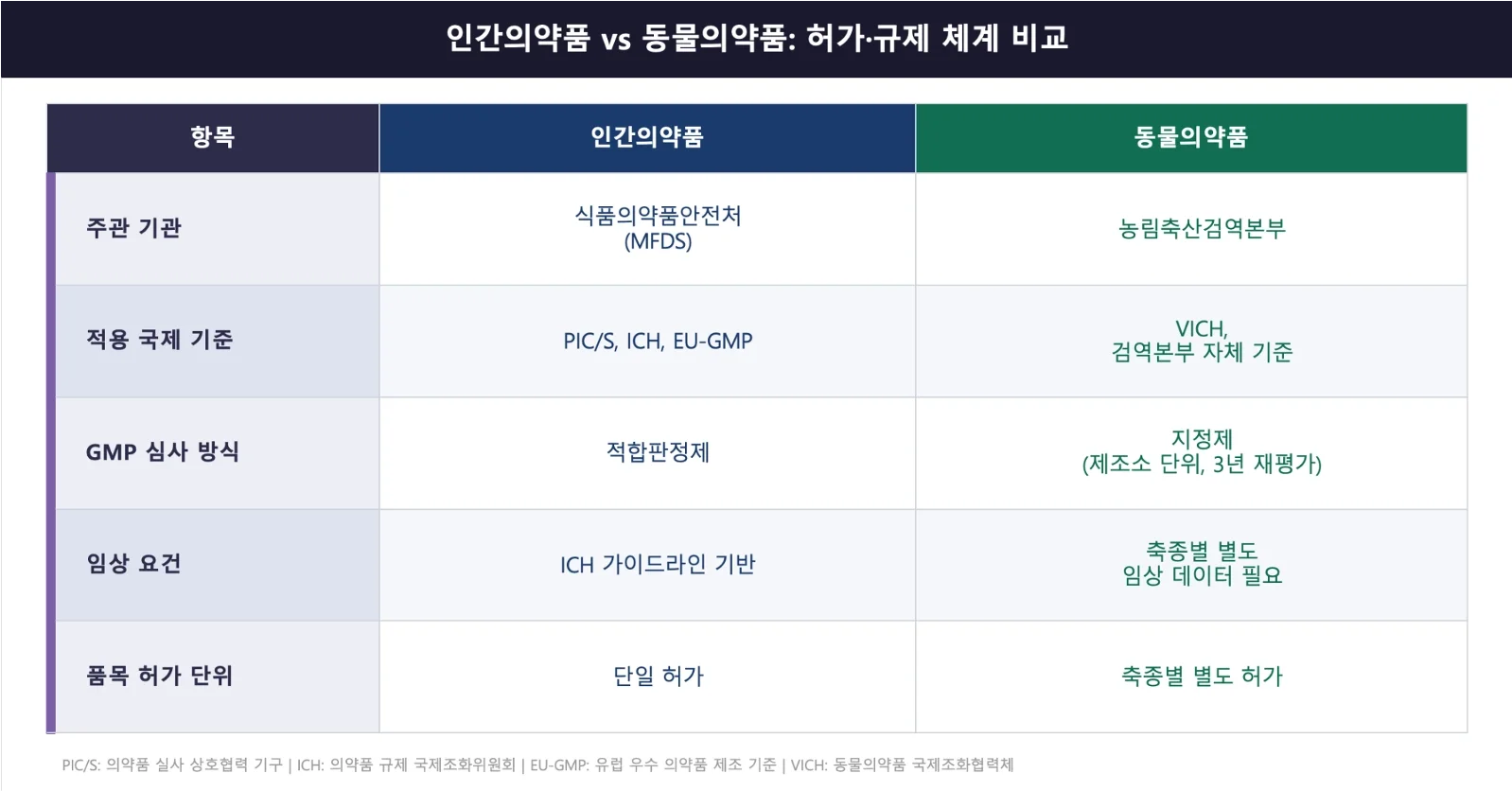
표에서 보듯 허가 단위도 다르다. 인간의약품은 성분·적응증 단위로 허가하지만, 동물의약품은 축종(種)별로 별도 허가가 필요하다. 같은 성분의 약이라도 '개용'과 '고양이용'은 다른 품목이다. 이것은 단순한 행정 절차의 차이가 아니라, 시장 진입 비용과 개발 우선순위를 결정하는 구조적 요인이다.
개발 속도는 더 빠르다
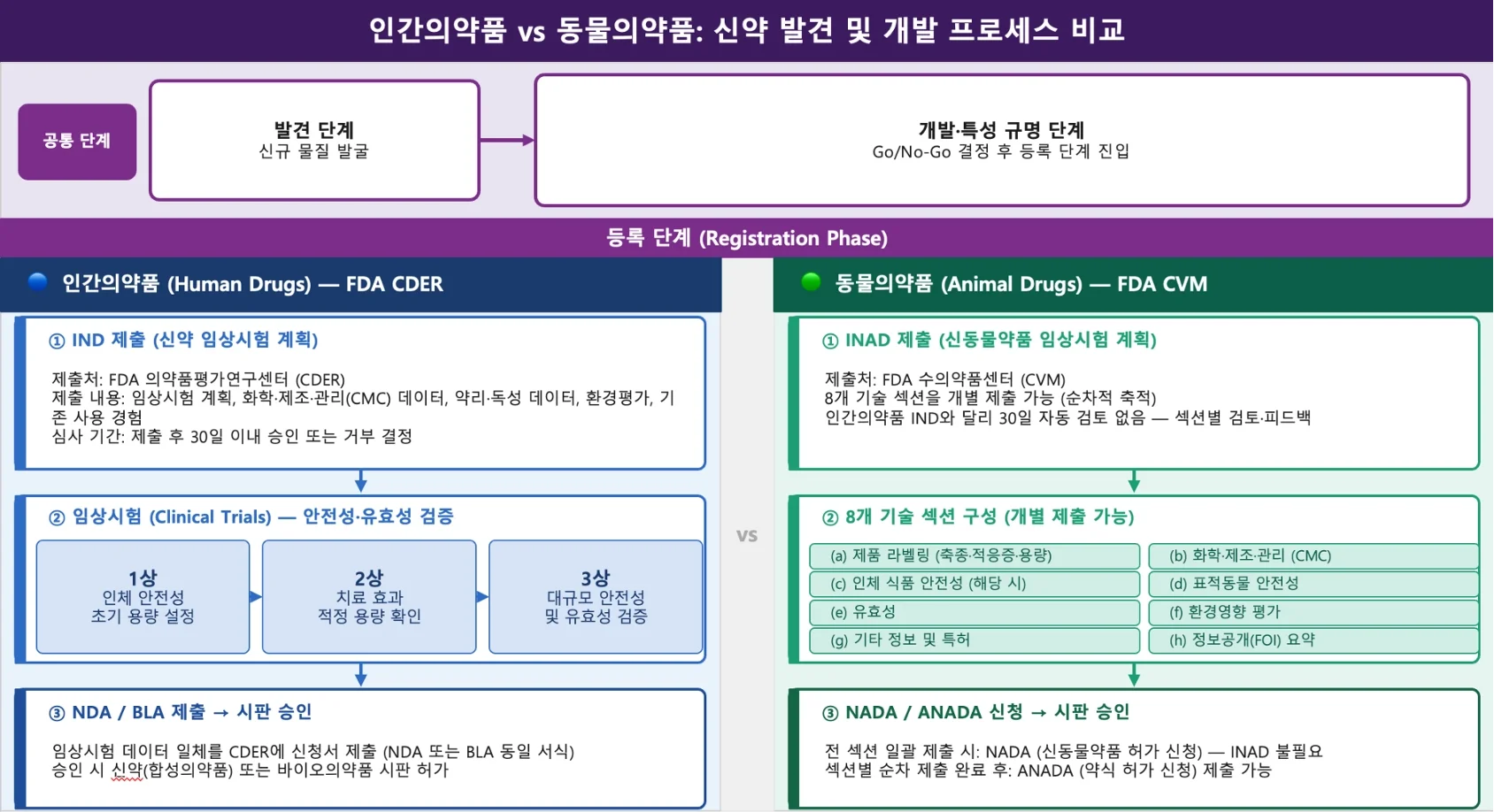
그림 3. 인간의약품, 동물의약품 신약개발 프로세스 비교 (출처: 식품의약품안전처, 농림축산검역본부, VICH 가이드라인 기반 필자 정리)
자료와 품목에 따라 차이는 있지만, 인간 신약은 통상 10년 이상 장기 개발과 대규모 임상 투자가 필요하다. 반면 동물의약품은 개발의 병목이 다르다. 인간의약품 개발이 ‘동물에서 사람으로’ 안전성과 유효성을 단계적으로 확장해가는 과정이라면, 동물의약품 개발은 처음부터 허가 대상 축종에서 실제
